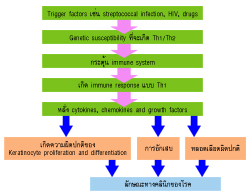
| ภูมิคุ้มกันของโรคสะเก็ดเงิน | ||||||||
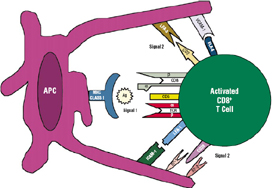
| Antigen presenting cell and T cell interaction | ||||||||
|
||||||||
| Cytokines | ||||||||
| ตารางที่ 3 แสดงชนิดของ cytokine ที่เพิ่มขึ้นในผื่นผิวหนังของผู้ป่วยโรคสะเก็ดเงิน | ||||||||
|
||||||||
| Keratinocyte | ||||||||
| |
||||||||
| Endothelial cell | ||||||||
| |
||||||||
| Neutrophil | ||||||||
|
||||||||