| การไม่ตอบสนองทางภูมิคุ้มกันต่อแอนติเจนของตนเอง
(Self tolerance) |
|
|
ในภาวะปกติ
ร่างกายมีกลไกหลายประการซึ่งมีความซับซ้อนมาก ที่จะควบคุมระบบภูมิคุ้มกันให้อยู่ในภาวะสมดุลย์
การควบคุมไม่ให้เกิดภูมิคุ้มกันต่อแอนติเจนของตนเอง ก็เป็นการทำงานที่สำคัญประการหนึ่งของระบบ
Immunoregulation เราเรียกภาวะไม่ตอบสนองต่อแอนติเจนของตนเองว่า Self-tolerance
ถ้ากลไกนี้มีความผิดปกติไป จะทำให้เกิดภาวะภูมิต้านทานต่อแอนติเจนตนเอง (Autoimmunity)
ขึ้นได้ ถ้าภาวะนี้ก่อให้เกิดพยาธิสภาพจนเป็นอันตรายต่อร่างกาย จะเรียกว่าเป็นโรคภูมิต้านเนื้อเยื่อของตนเอง
(Autoimmune Disease) จะเห็นว่าความเข้าใจเบื้องต้น ถึงระบบการควบคุมการตอบสนองทางภูมิคุ้มกันในภาวะปกติ
จึงมีความสำคัญมาก ทั้งเพื่อก่อให้เกิดความเข้าใจถึงพยาธิกำเนิดของโรค รวมทั้งเพื่อใช้ประโยชน์ในการรักษา
เช่น การชักนำให้เกิดภาวะ Self -tolerance กลับคืนมา ในโรคภูมิต้านเนื้อเยื่อของตนเอง
หรือการชักนำให้เกิด Acquired -tolerance ในการรักษาโรคภูมิแพ้ หรือใช้ในการเปลี่ยนถ่ายอวัยวะ
เป็นต้น
กลไกของ
Self-tolerance ที่สำคัญประกอบด้วย
|
| |
| 2.1
Central unresponsiveness หรือ Central tolerance |
| คือกลไกที่ใช้กำจัดลิมโฟไซท์ที่สามารถทำปฏิกิริยาต่อเนื้อเยื่อตนเองได้
โดยผ่านขบวนการ Negative selection ซึ่งเกิดขึ้นภายใน Central lymphoid tissues
เช่นในต่อมไทมัส และในไขกระดูก กลไกการทำลายของเซลล์นี้ เกิดขึ้นได้ทั้งกับ
T และ B lymphocytes โดยเกิดจากการที่เซลล์นั้นถูกทำลายไป (Clonal deletion)
หรือในบางกรณี เกิดจากการไม่ตอบสนองต่อแอนติเจน แต่ยังมีเซลล์นั้นปรากฏอยู่
(Clonal unresponsive หรือ Clonal anergy) ปัจจัยที่สำคัญสำหรับ ขบวนการ Intrathymic
selection ของ T lymphocytes คือโมเลกุลของ Self MHC ที่แสดงออกในต่อมไทมัส
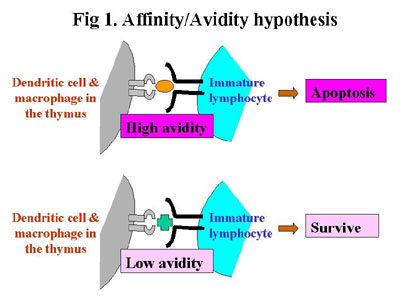
โดย T lymphocytes ที่จับกับ Self MHC ด้วย affinity หรือ avidity ที่สูงมากๆ
จะถูกทำลายไป ส่วนขบวนการ Negative selection ของ B lymphocytes เกี่ยวข้องกับการจับของ
แอนติเจนกับ Membrane IgM หรือ B cells Ig receptor ที่อยู่บนผิวของ B lymphocyte
โดยขึ้นกับ affinity, ชนิด, และปริมาณของแอนติเจน โดย B cells ที่จับกับ membrane-bound
self antigens ที่สามารถ Cross-link B cells Ig receptor ได้ด้วย avidity สูงๆ
จะถูกทำลายไป (Clonal deletion) (รูปที่ 1) |
| |
|
|
| |
| 2.2
Peripheral unresponsiveness หรือ Peripheral tolerance |
| ขบวนการ
Peripheral tolerance ประกอบไปด้วยกลไกอีกหลายประการ ที่ช่วยควบคุมการตอบสนองทางภูมิคุ้มกัน
หลังจากที่ลิมโฟไซท์ ออกมาจาก Central lymphid tissues แล้ว |
 2.2.1
Sequestered antigens 2.2.1
Sequestered antigens |
| กลไกหนึ่งที่ใช้อธิบายว่าทำไมร่างกายจึงไม่สร้างภูมิต่อเนื้อเยื่อบางชนิดในร่างกาย
เกิดขึ้นเนื่องจากการที่แอนติเจนของเนื้อเยื่อตนเองบางชนิด อยู่ในบริเวณที่ไม่ถูกรับรู้ด้วยเซลล์ของระบบภูมิคุ้มกัน
ซึ่งมีชื่อเรียกว่า บริเวณอภิสิทธิ์ทางภูมิคุ้มกัน (Immunological Privileged
site) โดยมักจะเป็นบริเวณที่ไม่มีเลือดหรือน้ำเหลืองไปเลี้ยงโดยตรง หรือมีสิ่งขวางกั้นอยู่
เช่น Blood brain barrier ทำให้แอนติเจนถูกนำเสนอต่อลิมโฟไซท์ หรือแมคโครฟาจ
ได้ยาก นอกจากนี้ จากการศึกษาเกี่ยวกับขบวนการ Apoptosis พบว่า เนื้อเยื่อในบริเวณเหล่านี้
มีการแสดงออกของ Fas ligand (FasL) จำนวนมาก ซึ่งอาจเป็นปัจจัยอีกประการหนึ่ง
ที่ทำให้ T cell ที่สามารถเข้าไปในบริเวณดังกล่าว ถูกทำลายด้วยขบวนการ Apoptosis
ผ่าน Fas-FasL ตัวอย่างเนื้อเยื่อที่จัดว่าเป็น Immunological Privileged site
ได้แก่ เนื้อสมอง, เชื้ออสุจิ, และ เลนส์ลูกตา เป็นต้น |
 2.2.2
การขาดสัญญาณที่สมบูรณ์สำหรับกระตุ้น T cells (Lack
of complete signal for T cell activation) 2.2.2
การขาดสัญญาณที่สมบูรณ์สำหรับกระตุ้น T cells (Lack
of complete signal for T cell activation) |
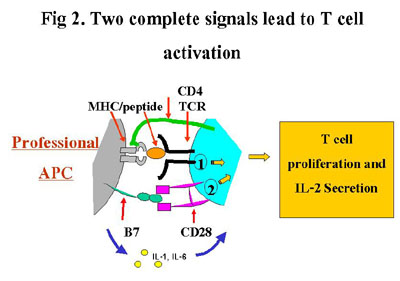
| ทฤษฏีที่ยอมรับกันมากในการกระตุ้น
T helper cell คือทฤษฏี "Two Signals model" ซึ่งกล่าวว่า ขบวนการกระตุ้น
T cell ให้ทำงานอย่างสมบูรณ์ จะต้องประกอบ ด้วยปฎิกิริยา ที่สำคัญสองชนิด (รูปที่
2) |
| |
|
|
| |
| นั่นคือ
1) ปฏิกิริยาระหว่าง T cell receptor ที่จะรับรู้ complex ของ antigenic
peptide กับ MHC class II molecule บนผิวของ APC โดยขั้นตอนนี้ เป็นตัวกำหนดการ
กระตุ้น T cell ให้มีความจำเพาะต่อทั้งแอนติเจนและ MHC และ 2) ปฏิกิริยาระหว่าง
Co-stimulatory molecule ต่างๆ จากโมเลกุลที่อยู่บนผิวเซลล์ เช่น B7, CD28,
CTLA-4 และจากลิมโฟไคน์ที่หลั่งจาก APC เช่น IL-1 และ IL-6 โดยปฏิกิริยาเหล่านี้
มีความสำคัญในการเสริมและคงไว้ ซึ่งการเชื่อมต่อระหว่างเซลล์ เพื่อให้เกิดการกระตุ้นของ
T cell อย่างสมบูรณ์ได้ รวมทั้งยังช่วยส่งสัญญาณ (Signal transduction) ที่จำเป็นต่อ
T cell อีกด้วย ดังนั้นในการกระตุ้นให้ T cell ทำงานได้อย่างสมบูรณ์นั้น จะต้องมีส่วนประกอบที่สำคัญดังกล่าวข้างต้นครบถ้วน
จึงเห็นได้ว่าเมื่อแอนติเจน ถูกนำเสนอบน professional APC เช่น แมคโครฟาจ หรือ
dendritic cell ใน Secondary lymphid organ ซึ่งเป็นบริเวณที่ T cell พบกับแอนติเจน
Professional APC ซึ่งมีการแสดงออกของ MHC class II และ co-stimulatory molecule
ที่ต้องการ ก็จะสามารถกระตุ้นให้เกิดการแบ่งตัว และการทำงานของ T cell ที่สมบูรณ์ได้
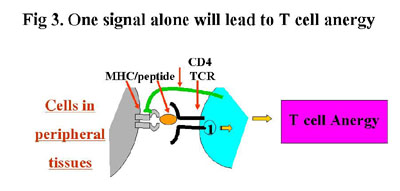
ในขณะที่ Autoantigen ซึ่งแสดงออกในอวัยวะอื่น และถูกนำเสนอให้กับ T cell โดยเซลล์ที่ขาดปัจจัยที่สำคัญ
เช่น ไม่มีการแสดงออกของ co-stimulatory molecules หรือ MHC molecule จะทำให้เกิดภาวะ
T cell anergy หรือ T cell unresponsiveness แทน (รูปที่ 3) ซึ่งเป็นกลไกของ
Self Tolerance ที่สำคัญมากประการหนึ่ง ที่เกิดขึ้นใน Peripheral tissue นอกจากนี้
เนื่องจาก T helper (TH) cell เป็นปัจจัยสำคัญต่อการการทำงานของ
B และ Cytotoxic T cell ภาวะ Anergy ของ TH cell จึงเป็นตัวกำหนดการทำงานของเซลล์ทั้งสองชนิดนี้ด้วย
|
| |
|
|
| |
 2.2.3
Immunoregulatory T cells/ Suppressor T cells 2.2.3
Immunoregulatory T cells/ Suppressor T cells |
เป็นเซลล์ที่มีคุณสมบัติยับยั้งการทำงาน
ของเซลล์ทางภูมิคุ้มกันชนิดอื่น กลไกการทำงานของ Suppressor T cells นี้ยังไม่เป็นที่เข้าใจ
อย่างชัดเจนในปัจจุบัน แต่เชื่อว่าเกิดจากการหลั่ง TGF-b
หรือ IL-10 ซึ่งมีฤทธิ์เป็น Inhibitory
cytokine |
 2.2.4
Idiotypic/ Anti-idiotypic network 2.2.4
Idiotypic/ Anti-idiotypic network |
|
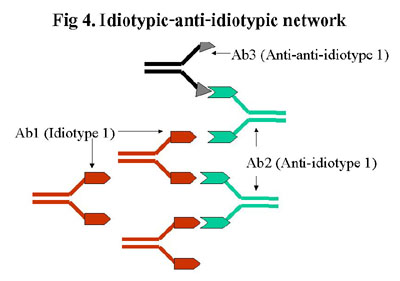
เกิดจากการสร้างแอนติบอดีต่อส่วน
idiotype ของแอนติบอดี จนเกิดเป็นเครือข่ายของปฎิกิริยาระหว่าง แอนติเจน-แอนติบอดีขึ้น
ตำแหน่งที่จะจับกับแอนติเจนบน Fab region ของ immunogobulin molecule หรือที่อยู่บน
T cell receptor เรียก "idiotype" ในสภาพปกติ แม้จะไม่มีแอนติเจนเข้าสู่ร่างกาย
ร่างกายก็มี idiotype อยู่ในระดับหนึ่ง แต่ถ้ามีแอนติเจนเข้ามาสู่ร่างกาย
ก็จะกระตุ้นให้มี idiotype ชนิดนั้นเพิ่มขึ้น idiotypeที่เพิ่มมากขึ้น จากการที่มีแอนติเจนเข้ามากระตุ้น
จะเสมือนหนึ่งเป็นสิ่งแปลกปลอม ถูกรับรู้ได้โดยระบบภูมิคุ้มกัน จึงเกิดการสร้างแอนติบอดีต่อ
idiotype (Ab1) ขึ้นเรียก anti-idiotype (Ab2), anti-idiotype เองก็เป็นสิ่งแปลกปลอม
ก็จะกระตุ้นให้เกิด anti-anti-idiotype (Ab3) ตามมา เป็นขั้นๆ ต่อไปเรื่อยๆ
(รูปที่4) "ทฤษฎี idiotype network" นี้ ตั้งขึ้นโดย Jerne เป็นอีกขบวนการหนึ่งที่สำคัญต่อการควบคุมภาวะภูมิคุ้มกันในร่างกาย
โดยผ่านปฏิกิริยาระหว่าง idiotype และ anti-idiotype บน immune cells
|
| |
|
|
|